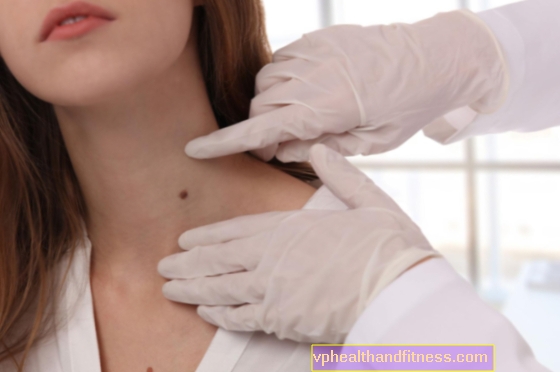
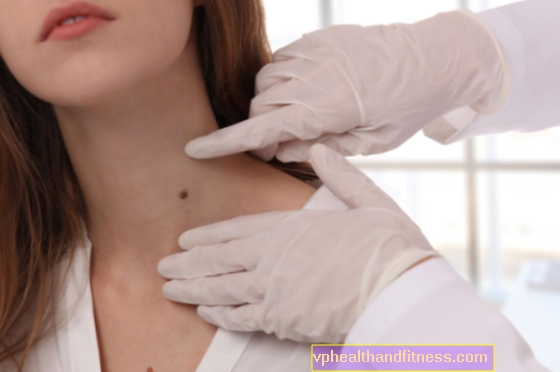
1 ml liuosta sisältää 1 mg galsulfaasia. Valmiste sisältää natriumia.
| Nimi | Pakkauksen sisältö | Vaikuttava aine | Hinta 100% | Viimeksi muokattu |
| Naglazyme | 1 valmistettava 5 ml: n injektiopullo ratkaisu inf. | Galsulfaasi | 2019-04-05 |
Toiminta
Lääke, joka vaikuttaa ruoansulatuskanavaan ja aineenvaihduntatuotteisiin. MPS VI on heterogeeninen ja monisysteeminen häiriö, jolle on tunnusomaista 4-sulfataasi-N-asetyyligalaktosamiinin, lysosomaalisen hydrolaasin, puute, joka katalysoi terminaalisten glykosaminoglykaanisulfaattidermaanisulfaattitähteiden hydrolyysiä. Entsyymiaktiivisuuden väheneminen tai puuttuminen johtaa dermataanisulfaatin kertymiseen monentyyppisiin soluihin ja kudoksiin. Hoidon perustana on palauttaa entsymaattinen aktiivisuus riittävä hydrolysoimaan kertynyt substraatti ja estämään sen jatkuva kertyminen. Cmax oli 2357 (± 1560) ng / ml, keskimääräinen T0,5 eliminoitumisvaiheessa oli 22,8 (± 10,7) minuuttia viikolla 24. Galsulfaasi käy läpi peptidihydrolyysin. Galsulfaasin erittyminen munuaisten kautta vaikuttaa vain vähän lääkkeen poistumiseen kehosta.
Annostus
Hoito on aloitettava mahdollisimman aikaisin ennen taudin peruuttamattomien kliinisten oireiden ilmaantumista. Hoidon tulee tapahtua lääkärin valvonnassa, jolla on kokemusta MPS VI: n tai muiden perinnöllisten metabolisten sairauksien hoidosta. Naglazyme tulisi antaa tarkoituksenmukaisessa kliinisessä ympäristössä siten, että hengenvaarallisten laitteiden käyttö on välittömästi mahdollista hengenvaarallisten hätätilanteiden hoitamiseksi. Suositeltu galsulfaasiannos on 1 mg / kg ruumiinpainoa. annetaan kerran viikossa laskimonsisäisenä infuusiona 4 tunnin aikana. Vanhukset: Valmisteen turvallisuutta ja tehoa ei ole varmistettu, eikä vaihtoehtoista annosteluohjelmaa varten ole suosituksia. Munuaisten ja maksan häiriöt: Valmisteen turvallisuutta ja tehoa ei ole arvioitu, eikä vaihtoehtoisille annosteluohjelmille näille potilaille ole suosituksia. Lapset ja nuoret: Ei ole erityisiä sääntöjä, jotka tulisi ottaa huomioon annettaessa valmistetta tälle potilasryhmälle. Antotapa: Alkuperäistä infuusionopeutta voidaan säätää siten, että noin 2,5% kokonaisliuoksesta annetaan tunnin aikana ja jäljellä oleva määrä (noin 97,5%) annetaan seuraavien 3 tunnin aikana. paino alle 20 kg, harkitse 100 ml: n infuusiopussien käyttöä. Tässä tapauksessa infuusionopeutta (ml / min) on pienennettävä siten, että infuusion kokonaiskesto on vähintään 4 tuntia.
Käyttöaiheet
Pitkäaikainen entsyymikorvaus potilailla, joilla on vahvistettu tyypin VI mukopolysakkaridoosin diagnoosi (MPS VI; N-asetyyligalaktosamiini-4-sulfataasin puutos; Maroteaux-Lamyn oireyhtymä). Hoidon perusta on alle 5-vuotiaiden nuorten potilaiden, joilla on vaikea sairaus, hoito, vaikka alle 5-vuotiaat potilaat eivät osallistuneet vaiheen 3 keskitutkimukseen. Alle 1-vuotiaista potilaista on vain vähän tietoja.
Vasta-aiheet
Akuutti tai hengenvaarallinen yliherkkyys vaikuttavalle aineelle tai jollekin apuaineelle, jos yliherkkyyttä ei voida hallita.
Varotoimenpiteet
Varovaisuutta tulee noudattaa rajoittavaa keuhkosairautta sairastavien potilaiden hoidossa ja hoidossa tai antihistamiinien ja muiden rauhoittavien lääkkeiden käytön huolellisessa seurannassa. Hengitysteiden positiivisen paineen käyttöä unen aikana ja trakeostomian mahdollisuutta kliinisesti sopivissa tilanteissa tulisi harkita. Lääkkeen infuusio saattaa olla tarpeen lykätä potilailla, joilla on akuutti kuumeinen sairaus tai hengitysvaikeuksia. Koska infuusioon liittyvät reaktiot (IAR), joiden ymmärretään tarkoittavan kaikkia infuusion aikana tai ennen infuusiopäivän loppua esiintyviä haittavaikutuksia, on suositeltavaa, että potilaat esilääkitetään antihistamiineilla yhdessä antipyreettien kanssa. tai ilman niitä, noin 30-60 min. ennen valmisteen infuusion aloittamista IAR-oireiden riskin vähentämiseksi. Harkitse IAR: n lieviä tai kohtalaisia oireita harkitsemalla antihistamiini- ja parasetamolihoitoa ja / tai pienentämällä infuusionopeus alle puoleen vasteenopeudesta. IAR: n yksittäisten vakavien oireiden tapauksessa infuusio on lopetettava, kunnes oireet häviävät, ja hoitoa antihistamiineilla ja parasetamolilla on harkittava. Infuusio voidaan aloittaa uudelleen 50-25%: lla nopeudesta, jolla se reagoi. Jos kyseessä on toistuva kohtalainen IAR-oire tai uudelleenkäsittely yksittäisten vaikeiden IAR-oireiden jälkeen, harkitse esilääkitystä (antihistamiineilla ja parasetamolilla ja / tai kortikosteroideilla) ja pienennä infuusionopeus 50-25%: iin edellisen vasteen nopeudesta. Vakavat allergiatyyppiset yliherkkyysreaktiot ovat mahdollisia, jos niitä esiintyy, on suositeltavaa lopettaa valmiste välittömästi ja toteuttaa asianmukainen hoito. Hätätilanteissa sovellettavia sääntöjä on noudatettava. Potilaita, jotka ovat kokeneet allergisen reaktion lääkkeen infuusion aikana, tulee yrittää uudelleen erityisen varoen; Erityisen koulutetun lääketieteellisen henkilöstön ja käytettävissä olevien elvytysvälineiden (mukaan lukien epinefriini) tulee olla läsnä antamisen aikana. Tämä akuutti tai mahdollisesti hengenvaarallinen yliherkkyys, jota ei voida hallita, on vasta-aihe lääkkeen uudelleentestaukselle. Valmiste sisältää natriumia - varovaisuutta on noudatettava potilaille, jotka noudattavat ruokavaliota, jonka natriumpitoisuus on rajoitettu. Selkäydinpuristus, myös kohdunkaulan alueella, ja myöhempi myelopatia on tunnettu ja vakava komplikaatio, jonka MPS VI saattaa aiheuttaa - potilaita tulee seurata selkäytimen kompression merkkien ja oireiden varalta (selkäkipu, halvaus painepisteen alapuolella, inkontinenssi virtsa ja ulosteet) ja tarvittaessa saa asianmukaista hoitoa.
Ei-toivottu toiminta
Hyvin yleiset: nielutulehdus, gastroenteriitti, arefleksia, päänsärky, sidekalvotulehdus, sarveiskalvon samentuma, korvakipu, kuulovamma, verenpainetauti, hengenahdistus, nenän tukkoisuus, vatsakipu, napanuorat, oksentelu, pahoinvointi, kasvojen turvotus, ihottuma nokkosihottuma, kutina, kipu, rintakipu, vilunväristykset, huonovointisuus, kuume, nivelkipu. Yleiset: kouristukset, hypotensio, apnea, yskä, hengitysvajaus, astma, bronkospasmit, punoitus. Tuntematon: anafylaktinen reaktio, sokki, parestesia, bradykardia, takykardia, syanoosi, kalpeus, kurkunpään ödeema, hypoksia, nopea hengitys.
Raskaus ja imetys
Lääkettä ei saa käyttää raskauden aikana, ellei se ole selvästi välttämätöntä. Imetys on lopetettava valmisteen käytön aikana. Lisääntymistutkimukset rotilla ja kaneilla, jotka saivat lääkettä enintään 3 mg / kg / vrk annoksina, eivät osoittaneet merkkejä heikentyneestä hedelmällisyydestä tai lääkkeen aiheuttamista haitallisista vaikutuksista sikiöön.
Valmiste sisältää ainetta: galsulfaasi
Korvaava lääke: EI






.jpg)